2026年衡水金卷先享题夯基卷地理Y1试卷,刷完这套地理卷,物质结构、有机推断再也不丢分!2026地理模考新题:实验操作+反应原理,全是高考常考!
10.C【解析】由图可知,每个晶胞中含有2个碘离子,钙离子的数目为(30°×二)×4+(36°×5×4=1,因此该物质的化学式是CaI₂,A项正确;碘化钙是离子晶体,熔融状态和水溶液中均可导电,B项正确;氟化钙和碘化钙均为离子化合物,阳离子相同,氟离子半径比碘离子半径小,因此氟化钙中阴、阳离子间作用力较强,熔、沸点较高,C项错误;s区H是非金属元素,D项正确。
二、非选择题
11.(20分)(1)[Ar]3d¹⁰4s¹(2分,其他合理答案也给分)(2)①小于(2分)②大于(2分)电负性:O>N,因此Cu²+与H₂O形成的配位键极性比Cu²+与NH₃形成的配位键要强,更易断裂,即Cu²+与NH₃的结合能力更强(2分)③ds(2分)N(2分)4(2分)④过氧化氢作氧化剂,氨与Cu²+形成配离子,两者相互促进使反应进行(2分,其他合理答案也给分)Cu+4NH₂·H₂O+H₂O₂—[Cu(NH₃)₄]²++4H₂O+2OH(2分)(3)
√398
(2分)
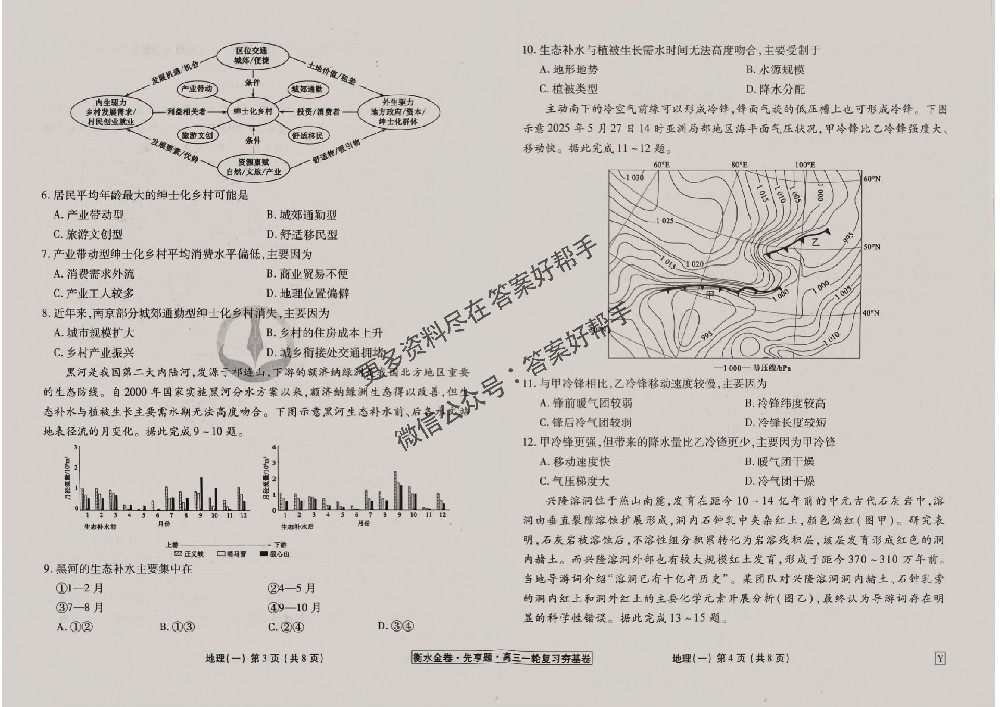
【解析】(1)基态Cu原子核外电子排布式为[Ar]3d¹⁰4s¹。(2)①NH₃价层电子对数为4,有1个孤电子对,为sp³杂化,NH4价层电子对数为4,没有孤电子对,为sp³杂化,由于孤电子对对键合电子对的排斥力比键合电子对之间的排斥力大,因此NH4的键角
更大。
②电负性:O>N.因此Cu²+与H₂O形成的配位键极性比Cu²+与NH₃形成的配位键要强,更易断裂,即Cu²+与NH₃的结合能力更强。
③[Cu(NH₃)₄]SO₄中Cu原子核外29个电子,价层电子排布式为3d¹⁰4s¹.属于ds区;[Cu(NH₃)₄JSO₄的内界离子是[Cu(NH₃)₄]²+,其中心Cu²-结合的配位体是NH₃,配位原子为N,Cu²~配位数是4。
④过氧化氢作氧化剂,氨与Cu²+形成配离子,两者相互促进使反应进行,反应的离子方程式为Cu+4NH·H₂O+H₂Oz=[Cu(NH₃)₄]²++4H₂O+2OH-。
(3)由均摊法可知,1个晶胞中Cu数目为8×8+6×—=4,C1数目为4,晶胞的质量为64×4+35.5×4g,晶胞的边长为,38cm.
2026年衡水金卷先享题夯基卷地理Y1试卷,2026地理模考新题:实验操作+反应原理,全是高考常考!刷完这套地理卷,物质结构、有机推断再也不丢分!
 衡水金卷先享题2025-2026答案帮-信息卷压轴卷
衡水金卷先享题2025-2026答案帮-信息卷压轴卷
